L’analyse céphalométrique est un examen permettant de mesurer avec précision les différents paramètres de la face, tant au niveau des dents que des os (basales et alvéolaires). Elle permet de quantifier les malocclusions et d’établir un diagnostic et un plan de traitement individualisé, adapté à chaque patient.
Le repérage des points anatomiques, des lignes, des plans et des mesures d’angles anatomiques sont réalisés sur chaque patient. Ainsi, nous possédons une connaissance parfaite de la morphologie propre de chacun de nos patients.
Les points médians
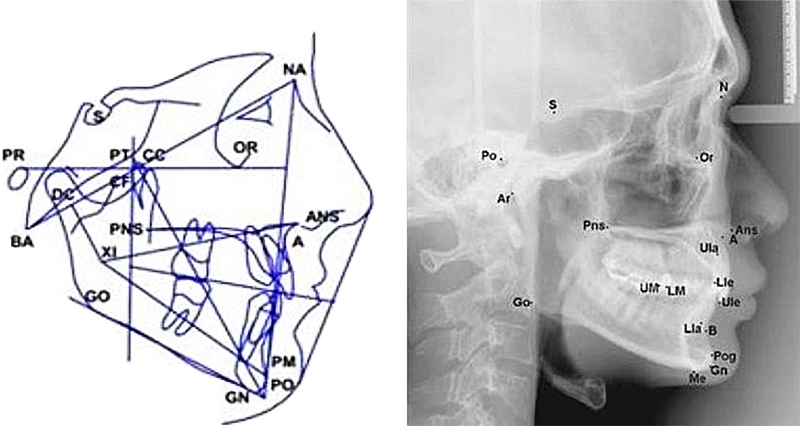 Fig. 01 : points céphalométriques réalisés avec le logiciel Cephio.
Fig. 01 : points céphalométriques réalisés avec le logiciel Cephio.
Ces points sont uniques et ont des dénominations bien précises :
• S : indique de l’image de la selle turcique.
• Na (qui signifie Nasion) : indique le point le plus antérieur de l’image de la suture fronto-nasale.
• ANS (aussi nommé ENA pour point Epine Nasale Antérieure) : indique le point le plus antérieur du prémaxillaire.
• PNS (aussi nommé ENP pour point Epine Nasale Postérieure) : indique le point le plus postérieur de l’image du palais secondaire.
• A (de DOWNS) : indique le point le plus postérieur de l’image de la concavité antérieur du prémaxillaire.
• Pr (qui signifie Prosthion) : indique le point le plus antérieur de l’image des procès alvéolaires supérieurs, entre les deux incisives centrales.
• I (point incisif supérieur) : indique le point le plus occlusal de l’image de l’incisive centrale supérieure.
• i (point incisif inférieur) : indique le point le plus occlusal de l’image des incisives inférieures
• id (point infradental ou point alvéolaire inférieur) : indique le point le plus antérieur de l’image des procès alvéolaires inférieurs entre les incisives centrales inférieures.
• B (de DOWNS) : indique le point le plus postérieur de l’image de la concavité antérieure de la symphyse mentonnière.
• Pog (qui signifie Pogonion) : indique le point le plus antérieur de l’image de la symphyse mentonnière.
• Me (qui signifie Menton) : indique le point le plus inférieur de l’image de la symphyse mentonnière.
• Gn (qui signifie Gnathion) : indique le point situé à mi-chemin entre Me-Pog.
• Ba (qui signifie Basion) : indique le point le plus inférieur de l’image du basi-occipital (ou point le plus antérieur du foramen magnum).
• P (aussi nommé PO pour Porion) : indique le point le plus supérieur de l’image du conduit auditif externe.
• GnCC (Gnathion Céphalométrique Construit) : indique le point situé à l’intersection du plan facial et du plan mandibulaire de DOWNS.
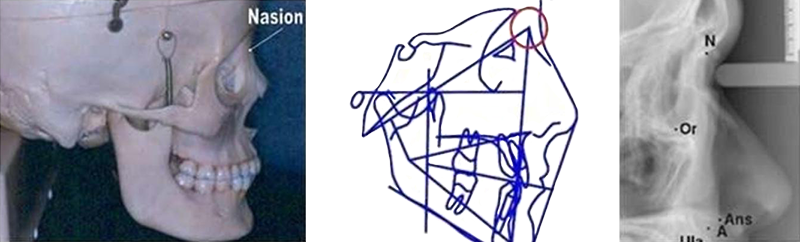
Fig. 02 : le point Na, le plus antérieur de l’image de la suture fronto-nasale.
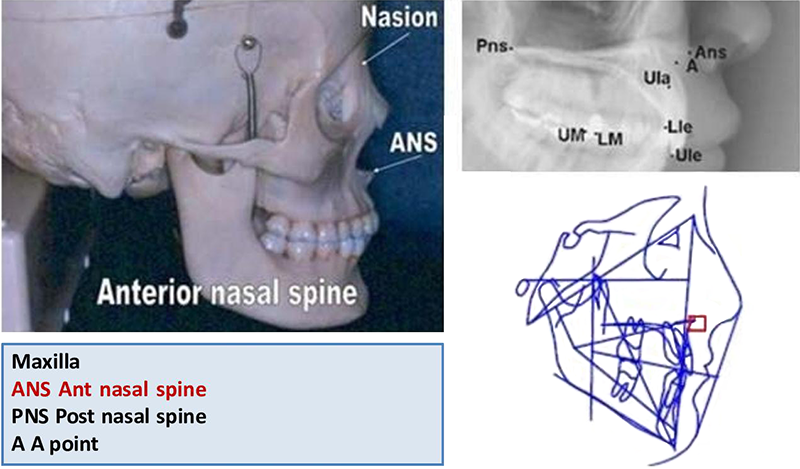
Fig. 03 : le point ANS, le plus antérieur du prémaxillaire.
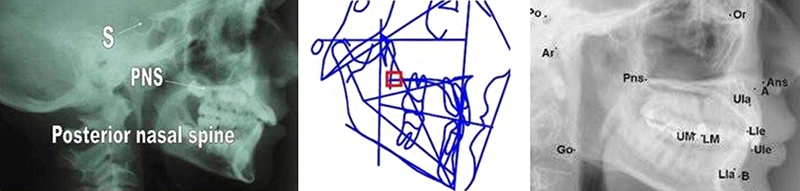
Fig. 04 : le point PNS, le plus postérieur de l’image du palais secondaire.
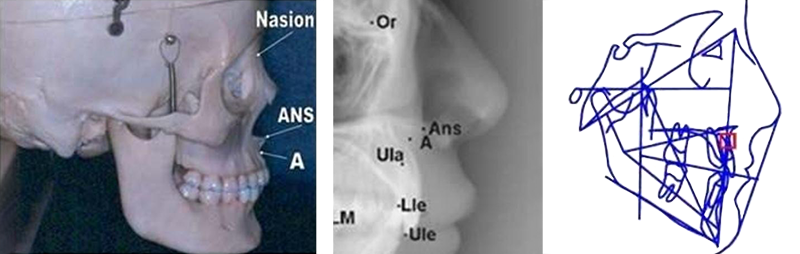
Fig. 05 : le point A, le plus postérieur de l’image de la concavité antérieur du prémaxillaire.
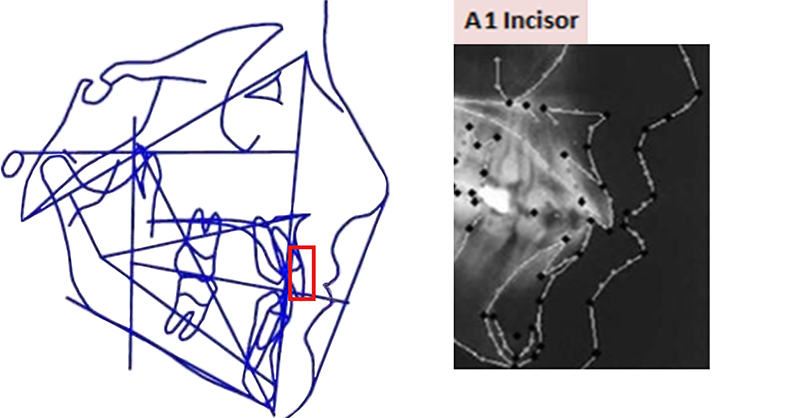
Fig. 06 : le point I, le plus occlusal de l’image de l’incisive centrale supérieure.

Fig. 07 : le point i, le plus occlusal de l’image des incisives inférieures.

Fig. 08 : le point B, le plus postérieur de l’image de la concavité antérieure de la symphyse mentonnière.
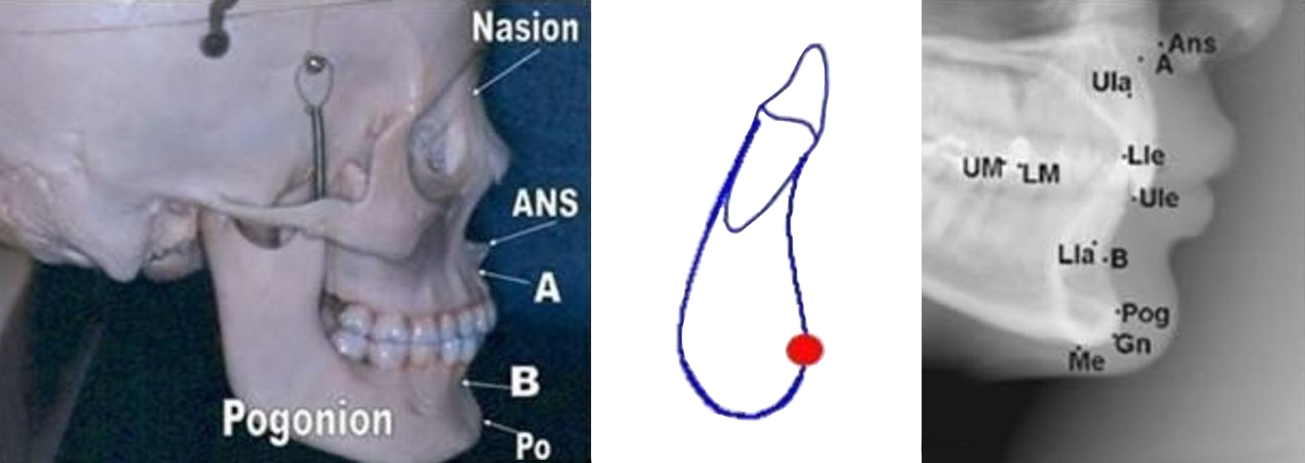
Fig. 09 : le point Pog, le plus antérieur de l’image de la symphyse mentonnière.
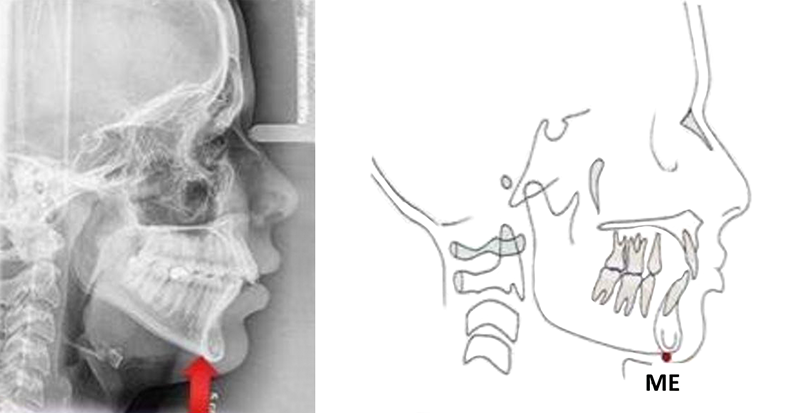
Fig. 10 : le point Me, le plus inférieur de l’image de la symphyse mentonnière.
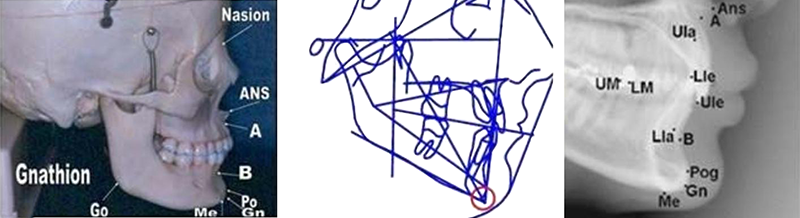
Fig. 11 : le point Gn est situé à mi-chemin entre Me-Pog.
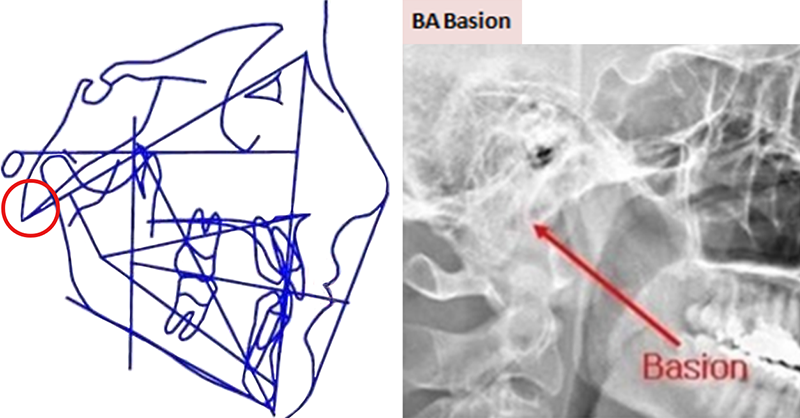
Fig. 12 : le point Ba, le plus inférieur de l’image du basi-occipital.
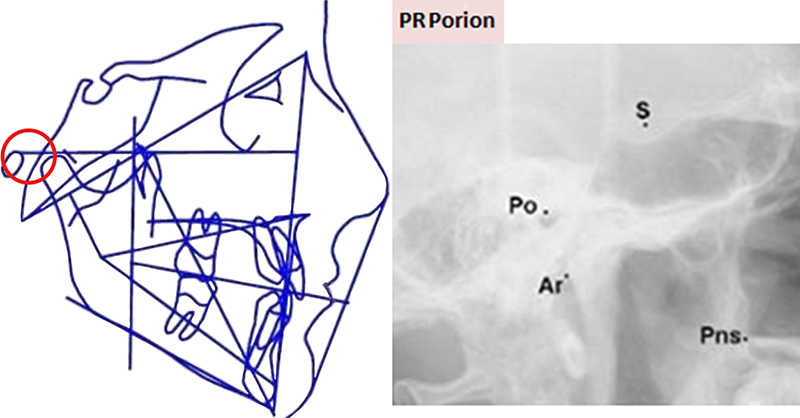
Fig. 13 : le point P, le plus supérieur de l’image du conduit auditif externe.




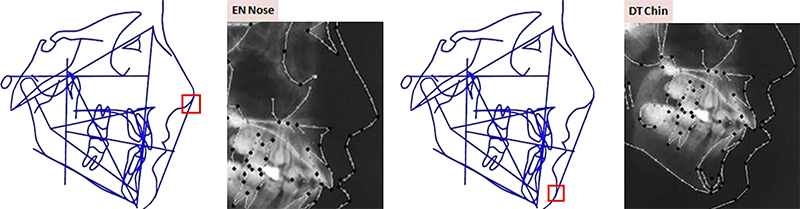


Fig. 14 : le point GnCC est situé à l’intersection du plan facial et du plan mandibulaire de DOWNS.
Les points bilatéraux
Ces points sont doubles :
• Or (qui signifie Orbital) : indique le point le plus inférieur de l’image du rebord externe de l’orbite.
• Pt (qui signifie Point ptérygoïdien) : indique le point d’entrée du canal grand rond dans l’arrière-fond de la fosse ptérygo-maxillaire ou le point à mi-chemin entre le point le plus supérieur et le point le plus postérieur de l’image de la fente ptérygo-maxillaire.
• Co (qui signifie Condylien) : indique le point le plus supérieur de l’image du condyle mandibulaire.
• Go (qui signifie Gonion) : point situé à mi-chemin entre la partie postérieure et la partie inférieure de l’angle mandibulaire.
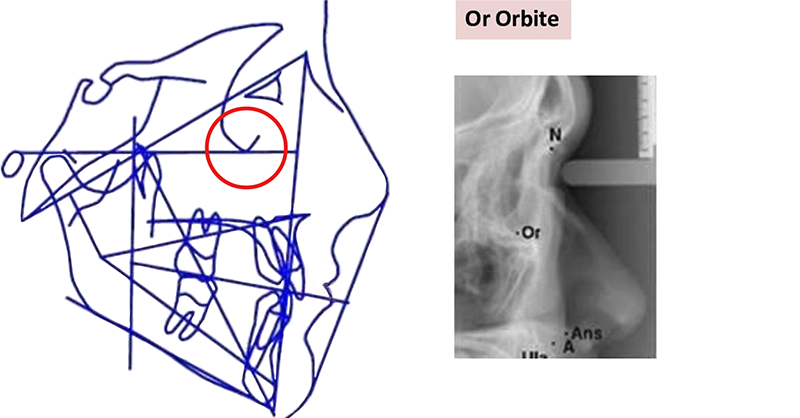
Fig. 15 : le point Or, le plus inférieur de l’image du rebord externe de l’orbite.

Fig. 16 : le point Pt, point d’entrée du canal grand rond dans l’arrière-fond de la fosse ptérygo-maxillaire ou point à mi-chemin entre le point le plus supérieur et le point le plus postérieur de l’image de la fente ptérygo-maxillaire.
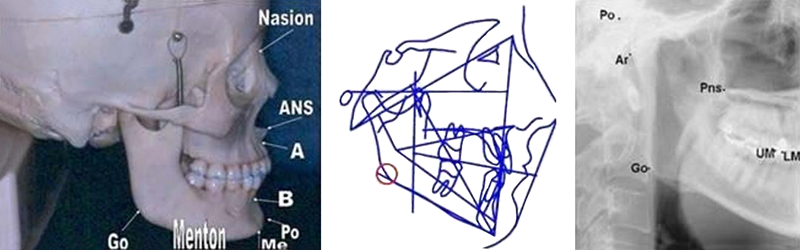
Fig. 17 : le point Go, point situé à mi-chemin entre la partie postérieure et la partie inférieure de l’angle mandibulaire.
Les plans horizontaux
Il existe 4 plans horizontaux lors d’une analyse céphalométrique :
• PHF (qui signifie Plan Horizontal de Francfort) : indique le plan qui passe par les deux porions et l’orbital gauche.
• Bispinal : indique le plan qui relie ENA à ENP. Ce plan est à peu près parallèle au PHF.
• Mandibulaire (de DOWNS) : indique le plan qui passe par Me et tangent dans la région de l’angle mandibulaire.
• Occlusal :
– Steiner : indique le plan bissectant les recouvrements molaires et incisifs.
– Ricketts : indique le plan bissectant les recouvrements molaires et canines ou molaires-prémolaires ou molaires-molaires temporaires. Ce plan permet de préciser où se situe la supraclusion (ou l’infraclusion) au niveau incisif.
Les lignes horizontales
En plus des 4 plans horizontaux présentés ci-dessus, on retrouve 2 lignes horizontales :
• S-Na : indique la ligne joignant S à Na.
• De la base du crâne : indique la ligne joignant Ba à Na.
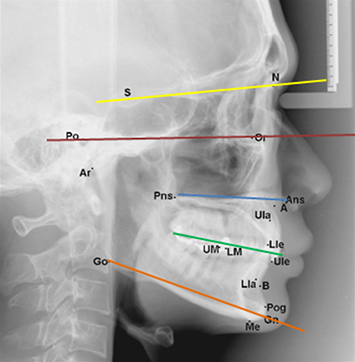
Fig. 18 : exemple de lignes horizontales.
Les plans verticaux
• Facial : indique le plan qui passe par Pog et Na.
• Ramal : indique le plan tangent au rebord postérieur du ramus (branche montante de la mandibule).
Les lignes verticales
• De Mac Namara : cette ligne est perpendiculaire au PHF passant par Na.
• De la denture : cette ligne joint Pog à A.
• E (ligne d’esthétique) : cette ligne joint la pointe du nez cutané au pogonion cutané.
• PtV (axe ptérygoïdien vertical) : cette ligne est perpendiculaire au PHF et passant par le point le plus postérieur de l’image de la fente ptérygo-maxillaire.
• Y (axe Y de Brodie) : cette ligne joint S à Gn.
• Axe facial (de Ricketts) : cette ligne joint Pt à GnCC ; cette ligne représente, comme l’axe Y, l’axe général de la croissance de la face.
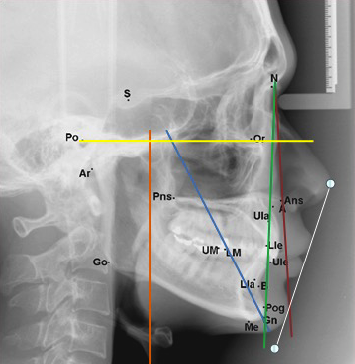
Fig. 19 : lignes verticales.
Vous pouvez voir la présentation complète du Dr Olivier Sandid au format numérique.
Références bibliographiques
O. Boury – L’analyse céphalométrique.
Site du cabinet d’orthodontie de Laon.
A. Lambert, O. Setbon, B. Salmon, V. Sebban – L’analyse céphalométrique.
[23-455-D-10] – Doi : 10.1016/S1283-0860(10)57179-3.
Points – Lignes – Plans.
Cecsmo, cours 6, traitement.
M. Rtibi, M. Nasfi, I. Medhioub, H. Gmati, A. Boughzela, A. Zinelabidine – Particularité céphalométrique des enfants ou jeunes patients avec hypertrophie des tonsilles palatines.
Le courrier du dentiste, 2022.